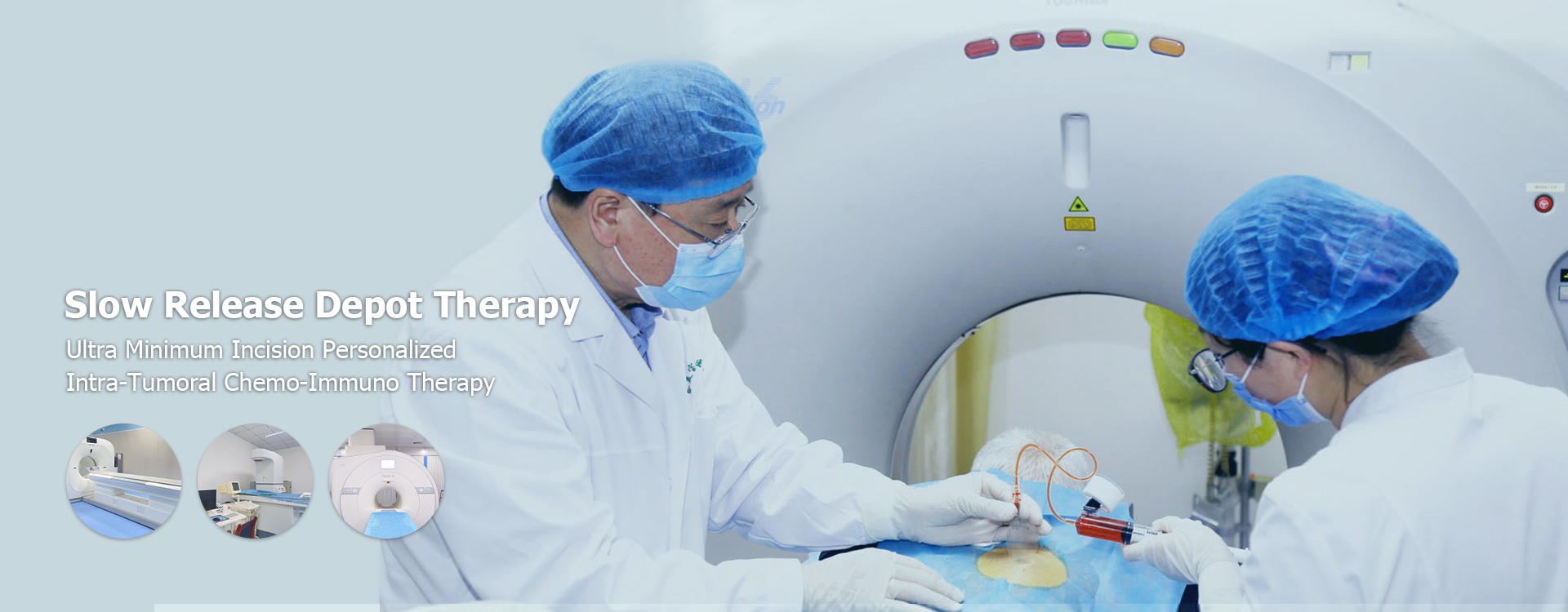
がん病院のためのローカライズされた薬物送達
がん病院のためのローカライズされた薬物送達
この記事では、の進歩と応用について説明しますローカライズされた薬物送達現代の癌病院の文脈内での癌治療のシステム。さまざまなテクニック、その利点、制限、将来の見通しを掘り下げ、腫瘍学の分野の専門家に包括的な概要を提供します。 提示された情報は、一般的な理解を提供することを目的としており、医学的アドバイスと見なされるべきではありません。
ローカライズされたドラッグデリバリーシステムの種類
標的ナノ粒子
ナノ粒子は、そのサイズとターゲティングリガンドで機能化する能力により、非常に正確な方法を提供しますローカライズされた薬物送達。 それらは、腫瘍部位に特異的に蓄積し、全身性毒性を最小限に抑えるように設計できます。 例には、リポソーム、ポリマーナノ粒子、および無機ナノ粒子が含まれます。 ナノ粒子の選択は、薬物溶解度、ターゲット特異性、望ましい放出動態などの要因に依存します。 腫瘍特異的抗原を利用するなど、改善されたターゲティングメカニズムの研究は、このアプローチの有効性を高め続けています。 特定のナノ粒子アプリケーションの詳細については、Nature NanotechnologyやACS Nanoなどのジャーナルで査読済みの研究を参照してください。自然ナノテクノロジーそしてACSナノ多くの場合、この分野で最先端の研究を特徴としています。
埋め込み可能な薬物送達システム
埋め込み型デバイスは、腫瘍部位で直接治療剤の持続的および制御された放出を提供します。 生分解性ポリマーや薬物溶出ステントなどのこれらのシステムは、薬物への長期暴露を提供し、投与の頻度を減らし、患者のコンプライアンスを改善します。 設計と材料の選択は、薬物放出のプロファイルと期間を決定する上で重要な要因です。 たとえば、ポリ(乳酸 - コグリコール酸)(PLGA)は、この目的のために一般的に使用される生分解性ポリマーです。Shandong Baofa Cancer Research Instituteそのような進歩をその治療計画に活用することができます。
標的抗体薬物コンジュゲート(ADC)
ADCは、モノクローナル抗体のターゲティング能力と化学療法薬の細胞毒性効果を組み合わせています。抗体は腫瘍細胞に特異的に結合し、ペイロードを標的に直接送達します。 このアプローチは、治療指数を大幅に強化し、ターゲット外の効果を最小限に抑えます。 多数のADCがFDAの承認を受けており、現在、さまざまな癌の臨床診療で使用されています。さらなる研究開発は、抗体工学、リンカー技術、ペイロードの最適化の改善に焦点を当て、さらに有効性と安全性を高めます。
ローカライズされた薬物送達における課題と将来の方向
薬剤耐性の克服
癌細胞はしばしば化学療法剤に対する耐性を発症します。 この課題を克服するための戦略の1つは、結合することですローカライズされた薬物送達相乗効果を生み出すために、免疫療法や放射線などの他の治療法で。 別のアプローチには、癌細胞のさまざまな経路を標的とする新規薬物の開発が含まれます。 この分野での研究は、の長期的な有効性を高めるために重要ですローカライズされた薬物送達戦略。
薬物浸透の改善
固形腫瘍への薬物の浸透は、腫瘍微小環境によって制限される可能性があります。腫瘍微小環境は、しばしば細胞外マトリックスと低酸素領域を備えていることがよくあります。 薬物浸透を強化する戦略には、これらの障壁を克服できるナノ粒子の使用、または腫瘍微小環境を修正して薬物送達を改善できるエージェントとの組み合わせが含まれます。
がん病院にローカライズされた薬物送達を実施する
実装の成功には、腫瘍医、薬剤師、エンジニア、研究者の間の学際的な協力が必要です。 病院は、これらの複雑なシステムの開発、製造、および管理をサポートするために、高度な技術とインフラストラクチャに投資する必要があります。 さらに、標準化されたプロトコルと品質管理措置は、の安全性と有効性を確保するために重要ですローカライズされた薬物送達治療。
の統合ローカライズされた薬物送達臨床診療には、患者の選択、治療計画、治療反応の監視など、さまざまな要因を慎重に検討する必要があります。継続的な研究開発は、患者の転帰を改善するために不可欠です。
結論
ローカライズされた薬物送達癌療法の重要な進歩を表しています。 課題は残っていますが、進行中のイノベーションはその有効性を高め、アプリケーションを拡大することを約束します。がん病院は、これらの進歩を改善された患者ケアに変換する上で極めて重要な役割を果たします。 がん治療の未来には、パーソナライズされた標的療法と標的療法のより大きな統合が含まれる可能性があります。ローカライズされた薬物送達このアプローチの基礎として。
関連している製品
関連製品