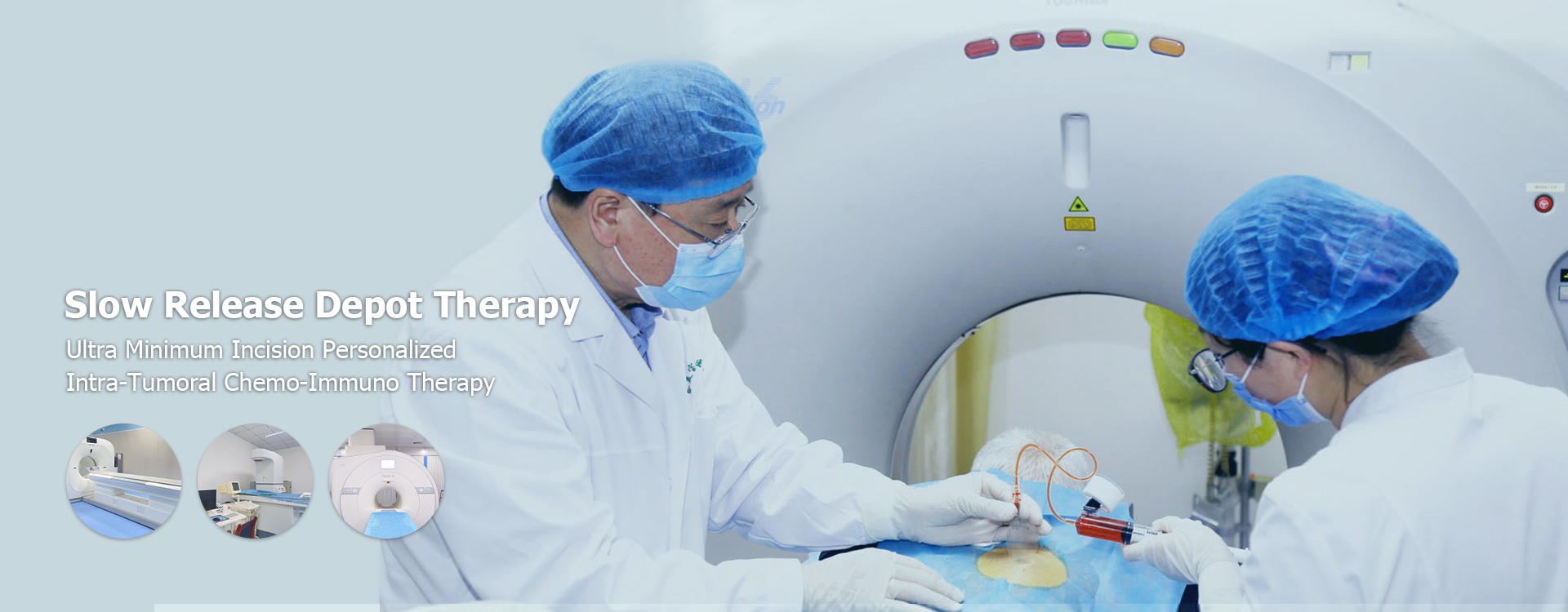
암 병원을위한 현지 약물 전달
암 병원을위한 현지 약물 전달
이 기사는 발전과 응용 프로그램을 탐구합니다현지화 된 약물 전달현대 암 병원의 맥락에서 암 치료 시스템. 우리는 다양한 기술, 이점, 한계 및 미래의 전망을 탐구하여 종양학 분야의 전문가를위한 포괄적 인 개요를 제공합니다. 제시된 정보는 일반적인 이해를 제공하기위한 것이며 의학적 조언으로 간주되어서는 안됩니다.
현지화 된 약물 전달 시스템의 유형
표적화 된 나노 입자
나노 입자는 크기와 표적화 리간드로 기능화하는 능력으로 인해 매우 정확한 방법을 제공합니다.현지화 된 약물 전달. 그것들은 종양 부위에 구체적으로 축적되어 전신 독성을 최소화하도록 설계 될 수 있습니다. 예는 리포좀, 중합체 나노 입자 및 무기 나노 입자를 포함한다. 나노 입자의 선택은 약물 용해도, 표적 특이성 및 원하는 방출 동역학과 같은 인자에 의존한다. 종양-특이 적 항원 사용과 같은 개선 된 표적화 메커니즘에 대한 연구는이 접근법의 효과를 계속 향상시킨다. 특정 나노 입자 응용에 대한 자세한 내용은 Nature Nanotechnology 및 ACS Nano와 같은 저널의 피어 검토 연구를 참조하십시오.자연 나노 기술그리고ACS 나노종종이 분야에서 최첨단 연구를 특징으로합니다.
이식 가능한 약물 전달 시스템
이식 가능한 장치는 종양 부위에서 직접 치료제의 지속 및 제어 방출을 제공합니다. 생분해 성 폴리머 또는 약물 제거 스텐트와 같은 이들 시스템은 약물에 장기간 노출되어 투여 빈도를 줄이고 환자 준수를 개선합니다. 설계 및 재료 선택은 약물 방출 프로파일 및 기간을 결정하는 데 중요한 요소입니다. 예를 들어, 폴리 (젖소-글리콜 산) (PLGA)는이 목적을 위해 일반적으로 사용되는 생분해 성 중합체입니다. 그만큼Shandong Baofa Cancer Research Institute치료 계획에서 이러한 발전을 활용할 수 있습니다.
표적화 된 항체-약물 접합체 (ADC)
ADC는 단일 클론 항체의 표적화 능력을 화학 요법 약물의 세포 독성 효과와 결합합니다. 항체는 특이 적으로 종양 세포에 결합하여 표적에 직접 페이로드를 전달한다. 이 접근법은 치료 지수를 크게 향상시켜 표적 외 효과를 최소화합니다. 수많은 ADC가 FDA 승인을 받았으며 현재 다양한 암의 임상 실습에 사용됩니다. 추가 연구 및 개발은 항체 공학, 링커 기술 및 페이로드 최적화를 개선하여 더 큰 효능과 안전성을 달성하는 데 중점을 둡니다.
현지화 된 약물 전달의 도전과 미래 방향
약물 내성 극복
암 세포는 종종 화학 요법 제에 대한 내성을 나타냅니다. 이 도전을 극복하는 한 가지 전략은 결합하는 것입니다현지화 된 약물 전달면역 요법 또는 방사선과 같은 다른 요법에서는 상승 효과를 만듭니다. 또 다른 접근법은 암 세포에서 다른 경로를 표적으로하는 새로운 약물의 발달을 포함한다. 이 분야의 연구는의 장기 효과를 향상시키는 데 중요합니다.현지화 된 약물 전달전략.
약물 침투 개선
고형 종양으로의 약물의 침투는 종양 미세 환경에 의해 제한 될 수 있으며, 이는 종종 조밀 한 세포 외 매트릭스 및 저산소 성 영역을 갖는다. 약물 침투를 향상시키기위한 전략에는 이러한 장벽을 극복 할 수있는 나노 입자의 사용 또는 약물 전달을 개선하기 위해 종양 미세 환경을 변형시킬 수있는 약제와의 조합이 포함됩니다.
암 병원에서 현지 약물 전달을 구현합니다
성공적인 구현에는 종양 전문의, 약사, 엔지니어 및 연구원 간의 학제 간 협력이 필요합니다. 병원은 이러한 복잡한 시스템의 개발, 제조 및 관리를 지원하기 위해 고급 기술 및 인프라에 투자해야합니다. 또한 표준화 된 프로토콜과 품질 관리 조치는의 안전성과 효능을 보장하는 데 중요합니다.현지화 된 약물 전달치료.
통합현지화 된 약물 전달임상 실습에 환자 선택, 치료 계획 및 치료 반응 모니터링을 포함한 다양한 요인을 신중하게 고려해야합니다. 지속적인 연구 개발은 분야를 진전시키고 환자 결과를 향상시키기 위해 필수적입니다.
결론
현지화 된 약물 전달암 요법에서 상당한 발전을 나타냅니다. 도전 과제는 여전히 남아 있지만 지속적인 혁신은 효능을 향상시키고 응용 프로그램을 확대 할 것을 약속합니다. 암 병원은 이러한 발전을 개선 된 환자 치료로 번역하는 데 중추적 인 역할을합니다. 암 치료의 미래에는 개인화되고 표적화 된 요법이 더 큰 통합이 포함될 것입니다.현지화 된 약물 전달이 접근법의 초석으로.
관련된제품
관련 제품